Résumé :
Les insomnies sont des pathologies du sommeil très fréquentes qui sont liées à différents facteurs physiologiques, psychologiques et environnementaux. La mélatonine, impliquée dans le mécanisme endogène de régulation du rythme veille-sommeil, est un traitement qui peut se révéler efficace contre les insomnies, mais une compréhension plus approfondie des patients est nécessaire pour une prise en charge adéquate.
Introduction : les insomnies
Les insomnies sont les troubles du sommeil qui touchent le plus grand nombre de personnes en France. Celles-ci peuvent avoir lieu au moment de l’endormissement, où la latence d’endormissement est allongée au-delà du seuil de 30 minutes considéré comme physiologique, au moment de micro-éveils nocturnes, les prolongeant ainsi, ou lors de réveils précoces. Elles sont dites primaires lorsqu’elles n’ont pas de cause sous-jacente et qu’elles ont lieu au moins trois fois par semaine pendant au moins 3 mois. Au-delà de cette période, elles sont considérées comme chroniques. Les insomnies dites comorbides sont liées à d’autres pathologies, notamment des troubles psychiatriques. Des facteurs psychologiques et environnementaux comme les traumatismes, les deuils, le stress, etc., vont aussi augmenter l’incidence de l’insomnie et parfois les perpétuer sur de nombreuses années.
Dans un nombre encore important de cas, les insomnies vont être prises en charge trop tardivement, voire jamais. Heureusement, la médecine du sommeil est de plus en plus médiatisée et les délais de prise en charge raccourcissent, car patients comme médecins ont une meilleure idée de la problématique.
Même si les approches non médicamenteuses restent la première intention pour les insomnies, certains traitements ont révélé leur efficacité, parmi lesquels la mélatonine.
La mélatonine endogène (Fig. 1)
La mélatonine est l’hormone dite de l’obscurité, qui gère en partie l’horloge du sommeil, la photopériode, mais elle ne déclenche pas le sommeil directement malgré son effet soporifique. Sa sécrétion déclenchée par l’obscurité induit de nombreuses modifications physiologiques, notamment en réduisant le taux de cortisol, des fonctions immunitaires ainsi que la température interne : les capillaires sanguins périphériques, au niveau de la peau et des extrémités, ont des récepteurs mélatoninergiques qui, sous l’action de l’hormone, vont être vasodilatés. Cela augmente l’afflux de sang périphérique et donc les échanges thermiques avec l’extérieur entraînant une baisse de la température du noyau interne central et améliorant ainsi la qualité du sommeil.
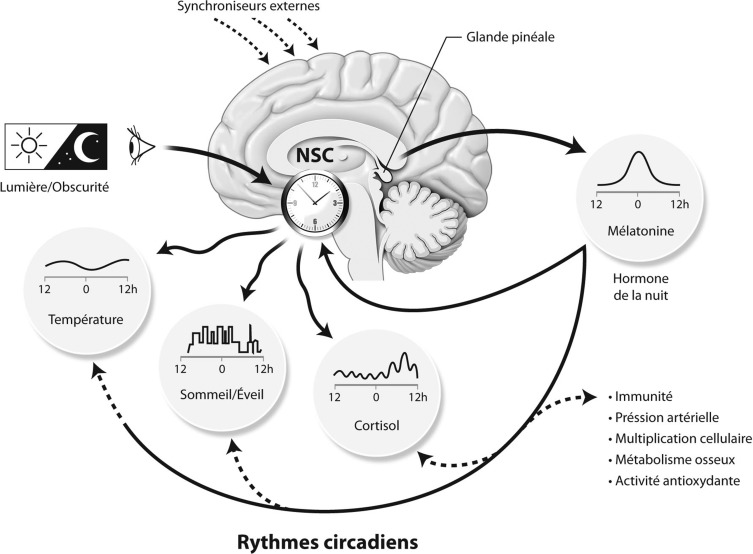
Figure 1 – Rythmes circadiens et mélatonine.
Métabolisme de la mélatonine
La mélatonine est une molécule chimiquement assez simple à fabriquer par l’organisme. Le tryptophane est le premier précurseur, qui va être métabolisé en sérotonine. Celle-ci est ensuite transformée en mélatonine en deux étapes qui nécessitent deux enzymes : la sérotonine-N-acétyltransférase (NAT), enzyme limitante de la synthèse de la mélatonine, et l’hydroxyindole-O-méthyltransférase (HIOMT). Au niveau cérébral, ce sont les pinéalocytes dans la glande pinéale qui la synthétisent. Celle-ci est sécrétée et utilisée en temps réel : contrairement à d’autres hormones comme le cortisol, la mélatonine n’est pas stockée dans des vésicules. Par conséquent, elle a une demi-vie courte, de 40-60 minutes en général, et elle est éliminée à 100 % de la circulation sanguine au bout de quelques heures.
La mélatonine exogène pour traiter les insomnies
Cette molécule peut être utilisée de manière exogène pour traiter les insomnies.
En France, la mélatonine est disponible sans prescription en parapharmacie à des doses inférieures à 2 mg (à la différence d’autres pays comme les États-Unis où la mélatonine en vente libre peut atteindre des posologies beaucoup plus élevées de 10, 15, voire 20 mg). Au-delà de 2 mg en France, une ordonnance est nécessaire. La mélatonine à libération prolongée (LP) est privilégiée pour faciliter l’endormissement et maintenir le sommeil en empêchant les éveils intra-sommeil nocturnes, car elle permet de limiter la dégradation trop rapide de la molécule limitant ses effets. Chez les sujets de 55 ans ou plus, la mélatonine LP améliore la qualité du sommeil, la vigilance matinale, la qualité de vie et diminue la latence d’endormissement, tant subjectivement qu’objectivement, parfois elle augmente la durée et l’efficacité du sommeil [1, 2].
C’est cette forme qui est intégrée dans les recommandations de l’AMM. La mélatonine à libération immédiate (LI) n’y est pas inscrite, mais dans la pratique elle peut fonctionner dans certains cas sur l’endormissement. Peu de travaux ont étudié le rôle de la mélatonine LI comme traitement de l’insomnie primaire.
Adaptation du traitement selon les profils
Le traitement doit être adapté, et parfois ajusté, selon différents facteurs notamment le type d’insomnie et l’âge. Le dosage n’est pas proportionnel à l’efficacité clinique : pour certains profils, une dose plus importante fonctionnera moins bien, voire pourra perturber davantage le sommeil. Même, dans certains cas, des petites doses de mélatonine peuvent aggraver les troubles du sommeil et la somnolence (effet de spillover). Il faut donc aller à l’encontre de la tendance à augmenter la dose en pensant que le traitement ne fonctionne pas et plutôt se tourner vers des microdoses.
Deux effets principaux sont distingués :
-l’effet chronobiotique, de régulation des cycles veille-sommeil, à faible dose (entre 0,5 et 2 mg). C’est l’effet recherché pour les personnes avec un décalage de phase. Pour les profils qui se couchent et se lèvent tard, en général des personnes jeunes, une dose administrée entre 4 et 6 h avant l’heure cible du coucher va induire, au bout de quelques semaines, une avance de phase de l’horloge interne. Chez les personnes, en général plus âgées, qui se couchent et se réveillent très tôt (par exemple, en présence d’un syndrome d’avance de phase 19 h-3 h), la mélatonine est administrée 11 h après le début de l’ascension de la sécrétion de mélatonine en lumière faible, le DLMO (Dim Light Melatonin Onset), qui est le marqueur le plus robuste et fiable de la phase circadienne.
-l’effet soporifique, à dose plus élevée entre 2 et 10 mg à prendre 30 à 60 minutes avant le coucher. La posologie est à adapter en fonction de différents paramètres, notamment la présence d’inducteurs ou d’inhibiteurs enzymatique et de l’âge, et à réadapter en fonction de l’efficacité chez le patient.
Cet effet est plutôt celui qui est recherché pour les patients ayant des difficultés d’endormissement en général.
Le traitement par mélatonine ne montre pas de perte d’efficacité liée à un effet d’habituation comme pour d’autres molécules où les doses doivent être augmentées régulièrement. La prise régulière d’une même dose est ce qui augmente le plus l’efficacité dans le temps.
Prise en compte du profil métabolique
Comme indiqué précédemment, le temps d’élimination de la mélatonine dans le sang est assez rapide. Cependant, ce temps est différent selon le profil métabolique des personnes : la dégradation hépatique de la molécule par les cytochromes 1A2 dépend notamment de leurs variants génétiques : certaines personnes métabolisent plus rapidement que d’autres ; 13 % de la population sont dits des métaboliseurs lents [3]. Cela aboutit à des taux sanguins endogènes variables d’une personne à l’autre (qui est par contre stable d’une nuit à l’autre pour une même personne à un moment donné de sa vie) ainsi qu’une réaction différente aux traitements par mélatonine exogène. Ces différences ne sont pas nécessairement corrélées à la qualité de sommeil, mais il est important d’en tenir compte lors des prises en charge.
Il est aussi important d’intégrer des facteurs qui peuvent agir sur le métabolisme, par exemple chez les personnes qui fument, les composés poly-aromatiques de la combustion du tabac stimulent le cytochrome 1A2 et accélèrent le métabolisme de la mélatonine. À noter aussi que ces enzymes métabolisent également la caféine. L’effet et la tolérance au café témoignés par un patient peuvent donc éventuellement servir d’indicateur indirect sur son métabolisme de la mélatonine.
Comorbidités et traitements
Les troubles du sommeil sont fréquemment liés à d’autres troubles avec lesquels ils s’auto-entretiennent, comme les troubles anxio-dépressifs, du spectre autistique (TSA), attentionnels avec ou sans hyperactivité (TDAH). Il est fondamental de prendre en compte ces comorbidités dans le traitement des insomnies.
–Pour les dépressions : les enregistrements de polysomnographie montrent des modifications de l’architecture du sommeil, notamment de la latence du sommeil paradoxal qui est raccourcie. Les troubles dépressifs provoquent fréquemment des insomnies à réveil précoce, et dans de plus rares cas de l’hypersomnie. La mélatonine à libération prolongée, permettant d’inhiber les micro-éveils nocturnes à l’origine des insomnies, peut donc se révéler efficace.
–Pour le TSA : la synthèse de mélatonine est retardée et chez 63 % des enfants avec TSA, les taux de mélatonine nocturne sont inférieurs à la moitié des taux moyens retrouvés dans le groupe sans TSA. La plus faible production de mélatonine était corrélée à la gravité des troubles autistiques (communication verbale et jeu). Pour les enfants atteints d’un TSA, le traitement des insomnies est effectué avec des comprimés de mélatonine particuliers recommandés par l’AMM, qui a une libération particulièrement prolongée de manière stable (Sylento® LP 1 ou 5 mg). L’amélioration de la qualité et la stabilité du sommeil chez les enfants TSA diminue les troubles neurodéveloppementaux, l’agitation, l’hypersensorialité et améliore l’apprentissage.
–Pour le TDAH : comme pour le TSA, la synthèse de mélatonine est retardée. Les personnes avec TDAH ont un retard de phase biologique avéré, avec une plage d’éveil maximale le soir, provoquant des activités éveillantes qui vont amplifier davantage le retard de phase. La dette de sommeil aggrave les troubles attentionnels, l’impulsivité et l’hyperactivité, ayant des répercussions comme l’absentéisme et l’échec scolaire chez les adolescents et jeunes adultes. En plus des traitements et approches thérapeutiques centrées sur le TDAH, remédier au décalage de phase avec la mélatonine peut s’avérer efficace.
Effets secondaires et cofacteurs
En l’état actuel des données scientifiques, la mélatonine est une substance active qui présente peu de risques sanitaires. Des effets secondaires consistent en des maux de tête, une frilosité, une perturbation du transit, car la mélatonine régule les rythmes de péristaltisme nocturne. Il faut cependant porter une attention particulière aux interactions avec des traitements avec l’antivitamine K (anticoagulant), la warfarine et la carbamazépine qui peuvent présenter des interactions délétères.
Comparée à d’autres traitements, notamment les benzodiazépines, la mélatonine ne présente pas d’effets secondaires comme la dépendance physiologique et le sevrage, les troubles cognitifs et de mémoire, l’augmentation du risque de chute et les apnées du sommeil.
Conclusion
La mélatonine peut donc se révéler très efficace dans différents cas pour traiter les troubles du sommeil avec peu d’effets secondaires. Un approfondissement systématique du profil de patient est important pour ajuster la prise en charge
La prise en charge non médicamenteuse
Les insomnies sont fréquemment liées à des éléments dits de cognition négative autour du sommeil, de rumination anxieuse, de croyances erronées du type « j’ai raté mon train du sommeil donc je ne pourrai plus m’endormir » ou « il faut absolument que je me sois endormi avant minuit ». Ces éléments de pensée sont autoréalisateurs des insomnies car ils déclenchent du stress et une anxiété de performance, alors que l’entrée dans le sommeil est un mécanisme de lâcher prise. L’anxiété va maintenir un niveau d’éveil élevé car le cerveau est incapable de différencier un stress réel issu de l’environnement d’un stress psychologique. De plus, rétroactivement, le cerveau va mémoriser les épisodes où la personne était couchée mais éveillée, avec une valence émotionnelle négative, ce qui va conditionner le développement d’une hypervigilance au moment du coucher et faire perdurer la répétition des mécanismes de l’insomnie. Pour traiter les insomnies primaires, le gold standard reste les thérapies cognitivo-comportentales qui peuvent être ajustées spécifiquement pour les insomnies (TCCI). De manière générale, les mécanismes les plus exploités sont les approches comportementalistes qui visent à contrôler les stimuli et restreindre le temps passé au lit. Par exemple, chez les personnes qui ont des difficultés à s’endormir, il est fréquemment demandé de retarder l’heure du coucher pour augmenter la dette de sommeil, ce qui a également pour effet de focaliser le patient sur le fait de rester éveillé et non sur l’injonction de devoir s’endormir, et donc de dormir plus facilement. Cela est aussi associé à la mise en place d’un rituel positif sur le sommeil, avec des activités calmes et apaisantes. Mettre en place une heure de lever régulière et stable, aussi bien sur les périodes personnelles que professionnelles, aide à obtenir des rythmes de veille-sommeil réguliers et de meilleure qualité.
Sommeil et lumière bleue
La lumière bleue, de longueur d’onde autour de 460 nm, a un effet éveillant en augmentant les taux de sérotonine et en inhibant la synthèse de mélatonine en stimulant la mélanopsine, pigment très présent sur les cellules rétiniennes de la couche ganglionnaire de la rétine impliquées dans le contrôle de l’horloge interne. En quelques minutes d’exposition seulement, la synthèse de mélatonine va être inhibée, et ce, pendant une durée de 1 à 3 heures. Ce mécanisme, impliqué naturellement dans le rythme éveil-sommeil en fonction de l’alternance jour/nuit, va également réagir aux sources de lumière artificielle, surtout à celles qui sont particulièrement riches en lumière bleue, notamment les interfaces digitales. Il est important de noter qu’en fonction du dispositif, la perturbation va être plus ou moins élevée. L’effet de la lumière sur la surface de la rétine suit la loi de l’inverse du carré de la distance : un lux est l’équivalent de l’énergie produite par un lumen incident sur une surface de 1 m2. Ainsi, à même intensité, si la distance de la source lumineuse est multipliée par deux, l’effet de la lumière sur la rétine est divisé par 4, une source de lumière à 1 mètre de distance (une télévision) aura un effet environ 10000 fois moins fort qu’une source à 10 cm de distance (téléphone portable).
Références :
1. Lemoine P, Nir T, Laudon M, Zisapel N. Prolonged-release melatonin improves sleep quality and morning alertness in insomnia patients aged 55 years and older and has no withdrawal effects. J Sleep Res 2007 ; 16 : 372-80.
2. Luthringer R, Muzet M, Zisapel N, Staner L. The effect of prolonged-release melatonin on sleep measures and psychomotor performance in elderly patients with insomnia. Int Clin Psychopharmacol 2009 ; 24 : 239-49.
3. Butler MA, Lang NP, Young JF et al. Determination of CYP1A2 and NAT2 phenotypes in human populations by analysis of caffeine urinary metabolites. Pharmacogenetics 1992 ; 2 : 116-27.



